はじめに
Fura 2-AM は最も使用頻度の高い細胞内Ca2+ 測定試薬です。その蛍光特性は、カルシウムイオン濃度が高くなると340 nm 励起の蛍光強度が上昇し、380 nm 励起の蛍光強度が低下します。そのときの蛍光強度比(R=Fex340nm/Fex380nm) をとると、色素の濃度、光源の強度、細胞の大きさ等に関係なくカルシウムイオン濃度と対応づけることができます。
Calcium Kit - Fura 2 は、Fura 2-AM と細胞内Ca2+ 測定に必要なBuffer 等を組み込んだスクリーニングキットです。細胞種や添加する薬剤などに応じて、Pluronic® F-127 またはCremophor® EL(Fura 2-AM の溶解補助剤)、Probenecid(陰イオントランスポーターの阻害剤)の各濃度を任意に設定できます。ハイスループットスクリーニングに用いられる各種蛍光プレートリーダーやインジェクターを備えた蛍光プレートリーダーにてリアルタイムで測定可能です。
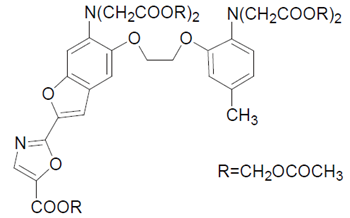
Fura 2-AM
キット内容
-
Fura 2-AM 50 μg x 10 Dimethylsulfoxide 2 ml x 1 Recording Medium (2X) 100 ml x 1 250 mmol/l Probenecid 1.3 ml x 1 5% Pluronic® F-127 2.5 ml x 1 5% Cremophor® EL 2.5 ml x 1
-
- 必要に応じて細胞洗浄用のPBS をご用意下さい。
キットには組み込まれておりません。 - 96 穴プレート10 枚分の測定が可能です。
- 必要に応じて細胞洗浄用のPBS をご用意下さい。
保存条件
冷凍にて保存してください。ご購入後、1 年以内にご使用ください。
使用上の注意
- Loading Buffer 及びRecording Medium は、用時調製してください。
- Loading Buffer は、長期保存すると、Fura 2-AM が分解する可能性があるので、出来るだけ1 回の操作で使い切ることをお薦めします。
- 励起波長340 nm/380 nm を使用出来るプレートリーダーをご使用下さい。
- 装置によっては、二波長同時測定ができないあるいは、340 nm/380 nm 励起ができない場合があります。
その場合は、姉妹品「Calcium Kit - Fluo 4」のご使用をお薦めいたします。
- 本製品には、ガラス製容器を使用しております。保護手袋を着用するなど、お取扱に際してはご注意ください。
プロトコール
1. 細胞の培養
マイクロプレートの各ウェルに細胞浮遊液を分注し、炭酸ガスインキュベーター内で一晩培養する。
- 付着細胞を使用する際は、96 穴プレートでは15,000 〜40,000 cells/well、384 穴プレートでは5,000 〜 15,000 cells/well 程度の細胞を一晩培養して使用することをお薦めします。
- 培養に用いる培地の量は、96 穴プレートで100 μl/well、384 穴プレートで25 μl/well をお薦めします。
2. Loading Buffer の調製 (96 穴マイクロプレート 1 枚分)
- 添付のDimethylsulfoxide から 50 μl を分取し、Fura 2-AM 1 本(50 μg)に加え、よく溶解する。
- 10 ml スケールの容器を準備する。Recording Medium(2X)5 ml を取り、測定条件に応じて、任意の量※の5% Pluronic® F-127(または5% Cremophor® EL)、250 mmol/l Probenecid を添加し、これに全量が10ml となるように純水を加え、よく混合する(本キットは予め、測定に最適なpH7.4 付近となるよう構成してあります)。
- Fura 2-AM のDimethylsulfoxide 溶液(50 μl) を添加して、超音波などでよく溶解し、Loading Buffer とする。
- 推奨濃度をProbenecid: 1.25 mmol/l 、Pluronic® F-127: 0.04 % としてありますが、濃度の変更は可能です。
Loading Buffer 10 ml を調製する場合、Probenecid、Pluronic® F-127 ( またはCremophor® EL) のアッセイ時の最終濃度と、添加量の関係は次のようになります。
-
250 mmol/l Probenecid 溶液の添加量と最終濃度 添加量(μl) 20 30 40 50 60 最終濃度(mmol/l) 0.50 0.75 1.00 1.25 1.50
-
5% Pluronic® F-127 (5% Cremophor® EL) 溶液の添加量と最終濃度 添加量(μl) 20 40 60 80 100 最終濃度(%) 0.01 0.02 0.03 0.04 0.05
3. Recording Medium (1X) の調製 (96 穴マイクロプレート 1 枚分)
- 別途、10 ml スケールの容器を準備する。Recording Medium(2X)5 ml に、測定条件に応じて、任意の量※250 mmol/l Probenecid を添加し、これに全量が10 ml となるように純水を加え、よく混合する(本キットは予め、測定に最適なpH7.4 付近となるよう構成してあります)。
- 37℃ インキュベーター中で加温しておく。
- 推奨濃度をProbenecid: 1.25 mmol/l としておりますが、濃度の変更は可能です。
Recording Medium(1X)10 ml を調製する場合、Probenecid のアッセイ時の最終濃度と、添加量の関係は以
下のようになります。
| 250 mmol/l Probenecid 溶液の添加量と最終濃度 | |||||
| 添加量(μl) | 20 | 30 | 40 | 50 | 60 |
| 最終濃度(mmol/l) | 0.50 | 0.75 | 1.00 | 1.25 | 1.50 |
4. 細胞へのFura 2-AM のロード
- 細胞を傷つけないように培地を取り除いた後、96 穴プレートで100 μl/well、384 穴プレートで25 μl/well のLoading Buffer を、それぞれのウェルに加える(必要に応じて、Loading Buffer を添加する前に、37°Cに加温したPBS で細胞を洗浄して下さい)。
- 37°Cで1 時間、インキュベートする。
- 細胞を傷つけないようにLoading Buffer を取り除き、予め37°C に加温しておいたRecording Medium (1X) を、96 穴プレートで100 μl/well、384 穴プレートで25 μl/well ずつ加える(必要に応じて、Recording Medium を添加する前に、37°Cに加温したPBS で細胞を洗浄して下さい)。
- 薬剤添加による蛍光強度変化を、各種蛍光プレートリーダーで測定する。
( λex = 340 nm/380 nm, λem = 510 nm)
よくある質問/参考文献
CS23: Calcium Kit - Fura 2
Revised Jan., 05, 2024


 を押して省略できます。
を押して省略できます。