がんとグルタミン代謝
がん細胞では、グルタミンを基質にα- ケトグルタル酸を供給する経路である「グルタミノリシス」の亢進が知られており、これに関連して種々の報告がされています。
例えば、がん遺伝子である KRAS はグルコースとグルタミン代謝を制御しているとされ 1)、また、膵臓腺がんの亢進には低酸素状態がグルコースおよびグルタミン代謝の活性化に関係し 2)、更には、グルタミン代謝が乳がん細胞の侵襲性を促進させる 2)など、グルタミン代謝とがんの関わりを解明する研究が盛んに行われています。
下記に、がん細胞におけるグルタミン代謝と「低酸素」「オートファジー]に関する報告例を紹介します。
低酸素とがん
膵管腺がんにおける低酸素下での解糖系の亢進は、ヘキソサミン生合成および生存を維持
低酸素状態になった膵臓がん細胞は、生存と細胞増殖を維持するため、酸化的リン酸化を促進する遺伝子の阻害を介した解糖系遺伝子の転写を活性化する。
これは、低酸素誘導因子である HIF1 によって促進され、これにより、グルコース消費および乳酸産生が増加する。
また、ヘキソサミン生合成経路(HBP 経路)を活性化させ生存を維持しようとするため、グルタミノリシスが亢進する。グルコースおよびグルタミンを炭素源として使用する HBP 経路が活性化することで、タンパク質の O-GlcNAc 修飾が増加すること、さらに、低酸素状態下にある膵臓がん細胞が産生する乳酸が、隣接するがん細胞の成長を促進することにより、がん細胞の生存率および増殖が維持されることが示唆されている 3)。
グルタミン代謝とオートファジー
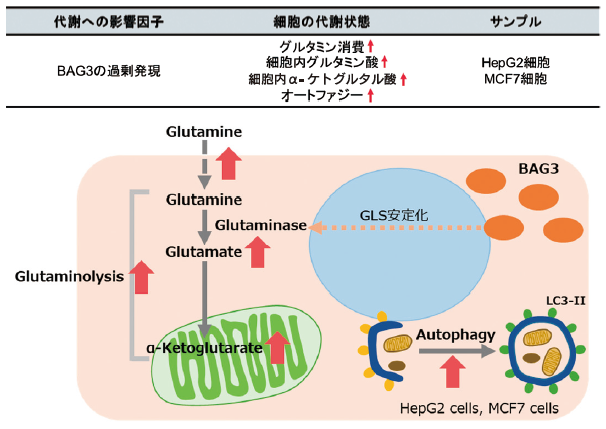
BAG3 によるグルタミナーゼの安定化を介したオートファジーとグルタミノリシスの促進
BAG3 は、アポトーシスや細胞分化、マクロオートファジー等の様々な細胞機能の制御に関与するタンパク質である。
BAG3 が過剰発現した細胞では、グルタミナーゼ(GLS)のスクシニル化が促進されることにより、ユビキチン化とそれに続くプロテアソーム分解が防がれ、GLS が安定化する。 GLS が安定化することで、グルタミン分解が促進されるため、グルタミン消費が亢進し、細胞内グルタミン酸およびグルタミン代謝産物である α- ケトグルタル酸が増加する。
グルタミン分解の促進により生じる培養液中のアンモニアは、オートファジーの活性化に寄与する。
グルタミノリシスが亢進しているがん細胞では、この
BAG3 ががん治療の標的になる可能性が示唆されている 4)。
関連製品情報
・グルタミン測定キット: P8, P13
・グルタミン酸測定キット: P8, P13
・オートファジー検出キット: P13
[参考文献]
1) Gaglio, D. et al., Mol. Syst. Biol., 2011, 7, 523.
2) Dornier, E. et al., Nat. Commun., 2017, 8, 2255.
3) Guillaumond, F. et al., PNAS, 2013, 110, 3919.
4) Zhao, S. et al., Cell Death & Disease, 2019, 284(10).