|
フェロトーシスは鉄依存性脂質過酸化によって引き起こされる制御された細胞死であり、虚血性臓器障害や神経変性疾患など多くの疾患と関係する重要な細胞死様式である。本研究は、ミトコンドリアダイナミクスがフェロトーシスの制御にどのように関与するかを解析したものである。解析の結果、フェロトーシス誘導時にはミトコンドリア分裂が促進される一方、ミトコンドリアダイナミクス関連因子であるDRP1やMitofusion1/2の発現抑制、またはOPA1の改変によってダイナミクスを阻害すると、フェロトーシスが抑制されることが明らかとなった。そのメカニズムとして、ミトコンドリア機能低下によりATP産生が減少し、AMP/ATP比の上昇によってAMPKが活性化される。活性化したAMPKは転写因子NRF2をリン酸化し核移行を促進する。NRF2はフェロトーシス抑制因子FSP1の発現を誘導し、脂質過酸化の抑制を介して細胞をフェロトーシスから保護する。さらに、ミトコンドリア融合促進因子M1は抗がん剤ドキソルビシンの抗腫瘍効果を維持しつつ化学毒性を軽減する可能性が示された。本研究はミトコンドリアダイナミクスが細胞死制御の重要な調節因子であることを示すとともに、薬剤性毒性を抑制する新たな治療戦略につながる可能性を示唆するものである。
|
|
Disrupting mitochondrial dynamics attenuates ferroptosis and chemotoxicity via upregulating NRF2-mediated FSP1 expression
論文へのアクセスはこちら: S. Ma., et al., Cell Report , (2025)
|
|
注目ポイント
・ミトコンドリアダイナミクス阻害によりAMPK–NRF2–FSP1経路が活性化し、脂質過酸化を抑えてフェロトーシス抵抗性が誘導される
・ミトコンドリア機能低下によるATP減少がAMPK活性化を引き起こし、細胞ストレス応答として抗フェロトーシス機構が作動する
・ミトコンドリア融合促進因子M1はドキソルビシンの抗腫瘍効果を損なわずに化学毒性を軽減する可能性が示された
|
| 関連製品 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| アプリケーションデータ |
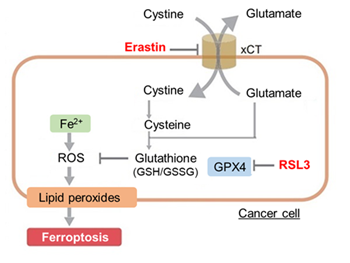
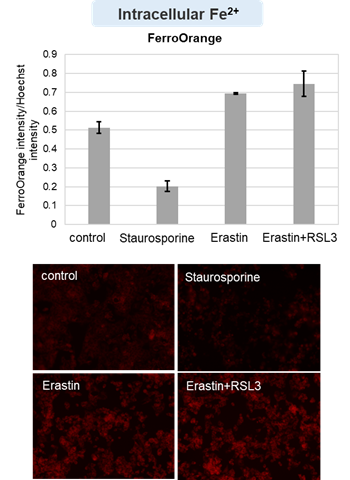
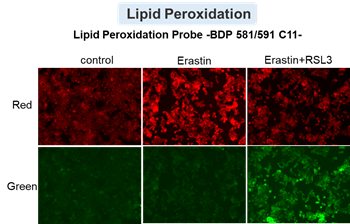
薬剤誘導による細胞死の各指標の変化:フェロトーシスとアポトーシスを見分ける
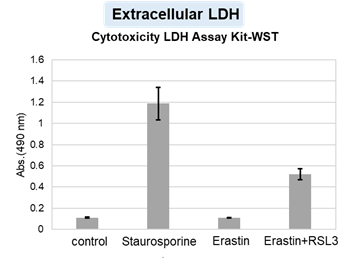
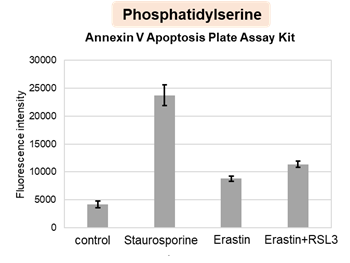
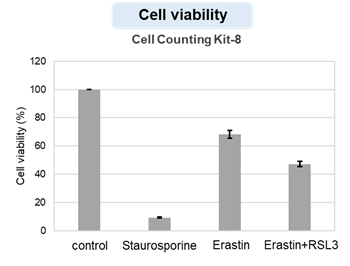
アポトーシス誘導剤であるStaurosporinまたはフェロトーシス誘導剤であるErastin、RSL3で処理したHepG2細胞の細胞外LDH、ホスファチジルセリン、細胞生存率、細胞内Fe2+、脂質過酸化の変化を解析しました。
その結果、Staurosporinで処理したアポトーシス誘導細胞ではホスファチジルセリンの増加、細胞生存率の低下並びに細胞外LDHが増加し細胞死が起きていることが確認できました。一方でフェロトーシス指標である細胞内Fe2+は変化がありませんでした。フェロトーシス誘導剤であるErastinで処理した細胞では細胞内Fe2+の増加と細胞生存率の低下が確認されましたが、細胞外LDHと脂質過酸化(脂質過酸化:赤色蛍光の減少と緑色蛍光の増加)は増加しませんでした。Erastinに加えてRSL3を同時に処理し、より強力にフェロトーシスを誘導した細胞では、フェロトーシスの指標である細胞内Fe2+と脂質過酸化の増加並びに細胞生存率の低下が確認され、死細胞が増加しました。一方で、ホスファチジルセリンはアポトーシス誘導細胞と比較し、フェロトーシス誘導時には増加率が低い結果となりました。これらの結果から、細胞死の指標を組み合わせて評価することで細胞死を見分けられることがわかりました。
<使用製品>
細胞外LDH :Cytotoxicity LDH Assay Kit-WST(製品コード:CK12)
ホスファチジルセリン:Annexin V Apoptosis Plate Assay Kit(製品コード:AD12)
細胞生存率 :Cell Counting Kit-8(製品コード:CK04)
細胞内Fe2+ :FerroOrange(製品コード:F374) *Hoechst 33342の蛍光強度で補正
脂質過酸化 :Lipid Peroxidation Probe -BDP 581/591 C11-(製品コード:L267)
<実験条件>
細胞:HepG2細胞(2×104 cells/well)
薬剤:Staurosporin(5 μmol/l), Erastin(25 µmol/l), Erastin+RSL3(どちらも25 µmol/l)
*無血清培地に希釈して添加
|
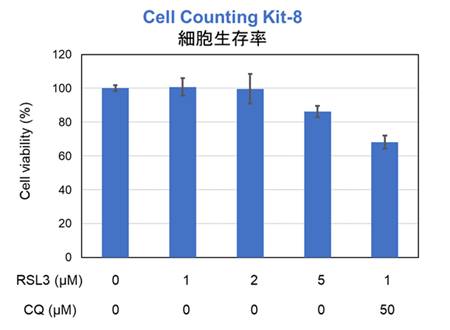
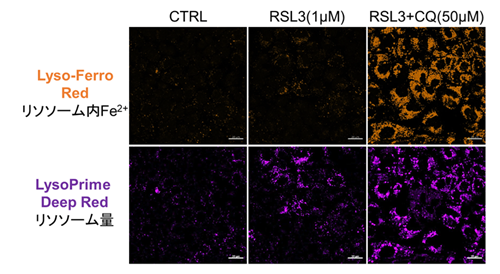
フェロトーシス誘導剤とリソソーム阻害剤の併用による各指標の変化
これまでがん細胞株間ではフェロトーシス感受性が異なることが示唆されており、フェロトーシス抵抗性のがん細胞においてリソソームのストレスを増加させることでフェロトーシスを促進できることが報告されている*。フェロトーシス抵抗性を示すがん細胞、A549細胞を用いてフェロトーシス誘導剤であるRSL3またはRSL3とリソソーム阻害剤であるChloroquine(CQ)を24時間処理し、細胞生存率、リソソーム内Fe2+、リソソーム量の変化を解析した。その結果、RSL3単独で処理した場合では細胞生存率、リソソーム内Fe2+に大きな変化はみられなかったが、一部リソソームが集積している様子(LysoPrime Deep Redの強い輝点)が観察された。一方、RSL3に加えてCQを同時に処理した細胞では、リソソーム内Fe2+の増加とリソソームの肥大化、細胞生存率が低下する既報と同様の結果が得られ、フェロトーシス促進にリソソーム内Fe2+の増加が関与している可能性が示唆された。
*Y. Saimoto, et al., Nature Communications, 2025, 16, 3554.
<使用製品>
リソソーム内Fe2+: Lyso-FerroRed (製品コード:L270)
リソソーム量:LysoPrime Deep Red (製品コード:L264)
細胞生存率: Cell Counting Kit-8 (製品コード:CK04)
|
Science Noteのバックナンバーはこちらから!