|
リソソームは従来、オートファジーを通じて炎症関連複合体を除去する役割をもつことで知られてきた。今回の論文は、それに加えてリソソーム自体が炎症シグナルを直接制御する機能をもつことを示した点で重要である。
焦点となるのは、リソソーム局在チャネルTRPML1だ。炎症刺激に伴うROS上昇でTRPML1が活性化されると、リソソーム内Fe2+の放出が促進され、プロリン水酸化酵素(PHDs)が活性化される。その結果、NF-κBの転写活性が抑えられ、IL1B転写とIL-1β産生が抑制される。つまり、TRPML1はマクロファージの過剰炎症に対する内蔵ブレーキとして働くのである。
さらに炎症性腸疾患(IBD)の代表的な実験モデルの一つであるDSS誘発性大腸炎モデルマウスにおいて、TRPML1作動薬ML-SA5の投与により生存率、体重減少、疾患活動性、結腸短縮、粘膜障害が改善した。IL-1βの補充によりML-SA5の保護効果は失われたことから、TRPML1活性化による抗炎症作用にはIL-1β抑制が重要な役割を果たすことが示唆された。これらの知見は、TRPML1を介したリソソームシグナルが腸炎制御に関与し、IBD関連病態に対する新たな治療標的となる可能性を示す。
|
|
Lysosomes finely control macrophage inflammatory function via regulating the release of lysosomal Fe2+ through TRPML1 channel
論文へのアクセスはこちら: Xing, Y., et al, Nat Commun., (2025)
|
|
注目ポイント
・リソソームは分解小器官にとどまらず、Fe2+シグナル制御を介して炎症転写を直接調節する場である。
・TRPML1活性化によりPHDs–NF-κB–IL-1β経路が抑制され、マクロファージの過剰炎症を防ぐ 。
・DSS大腸炎モデルでTRPML1作動薬が症状改善を示し、IBD治療標的としての可能性が示唆された。
|
| 関連製品 |
|
|
|
|
|
|
|
|
|
|
| アプリケーションデータ |
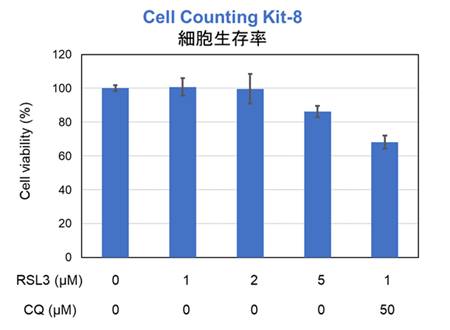
フェロトーシス誘導剤とリソソーム阻害剤の併用による各指標の変化
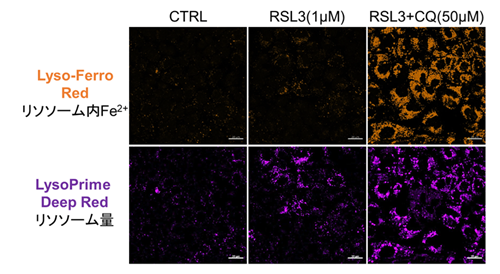
これまでがん細胞株間ではフェロトーシス感受性が異なることが示唆されており、フェロトーシス抵抗性のがん細胞においてリソソームのストレスを増加させることでフェロトーシスを促進できることが報告されている*。フェロトーシス抵抗性を示すがん細胞、A549細胞を用いてフェロトーシス誘導剤であるRSL3またはRSL3とリソソーム阻害剤であるChloroquine(CQ)を24時間処理し、細胞生存率、リソソーム内Fe2+、リソソーム量の変化を解析した。その結果、RSL3単独で処理した場合では細胞生存率、リソソーム内Fe2+に大きな変化はみられなかったが、一部リソソームが集積している様子(LysoPrime Deep Redの強い輝点)が観察された。一方、RSL3に加えてCQを同時に処理した細胞では、リソソーム内Fe2+の増加とリソソームの肥大化、細胞生存率が低下する既報と同様の結果が得られ、フェロトーシス促進にリソソーム内Fe2+の増加が関与している可能性が示唆された。
*Y. Saimoto, et al., Nature Communications, 2025, 16, 3554.
<使用製品>
リソソーム内Fe2+: Lyso-FerroRed (製品コード:L270)
リソソーム量:LysoPrime Deep Red (製品コード:L264)
細胞生存率: Cell Counting Kit-8 (製品コード:CK04)
|
Bafilomycin A1 によるオートリソソームの形成阻害の解析
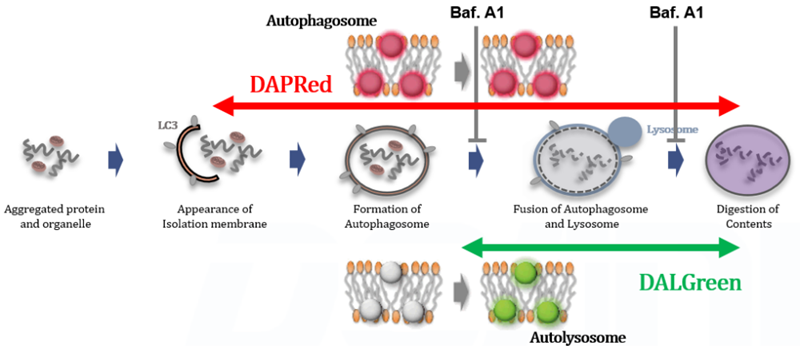
DALGreenおよびDAPRedで染色したHeLa細胞を用いて、リソソーム酸性化阻害剤バフィロマイシンA1(Baf.A1)により誘導されるオートファジーによる一連の流れの変化を評価した。飢餓状態と比較して、Baf.A1の添加によるオートリソソーム形成阻害条件下では、DALGreenの蛍光シグナルは減少した。一方、DAPRedの蛍光シグナルは同条件下で増加したことから、Baf. A1はオートファゴソームの蓄積を誘導した。
実験データ
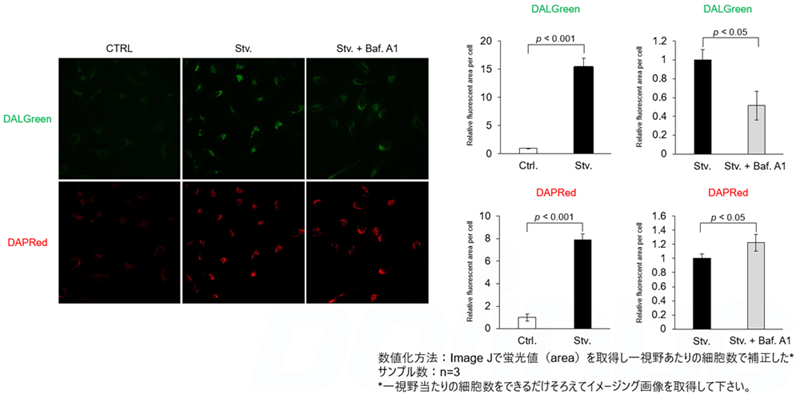
<実験条件>
CTRL: 通常培養条件、Stv.: 飢餓誘導条件、Baf. A1: オートリソソーム形成阻害条件
DALGreen検出条件: 488 nm (Ex), 490–550 nm (Em)
DAPRed検出条件: 561 nm (Ex), 565–700 nm (Em)
<使用製品>
Autophagic Flux Assay Kit
|
Science Noteのバックナンバーはこちらから!






























