|
パーキンソン病(PD)は、中脳の黒質緻密部(SNpc)のドーパミン作動性(DA)ニューロンの喪失によって引き起こされる加齢性運動障害ですが、PDにおけるこのDAニューロン喪失の根本的な原因は不明のままであり、PDの効果的な治療法は未だ確立されていない。最近の研究では、環境要因と遺伝的要因の両方がPD発症の基盤となっており、リソソーム機能不全と脂質蓄積が病気の進行に寄与していることが明らかになっている。本論文では、グルコシルセレミド(GluCer) の蓄積が DA ニューロンで細胞老化を直接誘発することを示し、老化細胞での ペリリピン(PLIN2) のアップレギュレーションは脂質蓄積を悪化させ、α-シヌクレイン 蓄積を促進し、PD における老化表現型および炎症老化を促進させ、それによって免疫反応依存性の DA ニューロンの喪失を増大させる可能性があることを明らかにした。これらの知見は、加齢に伴うリソソーム障害、脂質蓄積、およびDAニューロンの細胞老化が関連していることを示しており、これが中脳の炎症を引き起こし、最終的に神経変性とPDにつながる可能性を示唆している。 |
|||
|
Lipid accumulation drives cellular senescence in dopaminergic neurons |
|||
|
注目ポイント ・PDは、ドーパミン作動性ニューロンの喪失に関連しており、遺伝的および環境的要因がその進行に寄与している ・リソソーム酵素β-グルコセレブロシダーゼの変異は脂質の蓄積を引き起こし、PDにおけるドーパミン作動性ニューロンの細胞老化を促進する ・脂肪滴の凝集とリソソーム機能性傷害は、PDにおける神経変性につながる細胞老化の引き金となる可能性がある |
|||
| 関連製品 | |||
|
|||
|
|||
|
|||
|
|||
|
|||
| アプリケーションデータ | |||
固定化細胞を用いた脂肪滴染色と細胞老化アッセイ(イメージング) |
|||
|
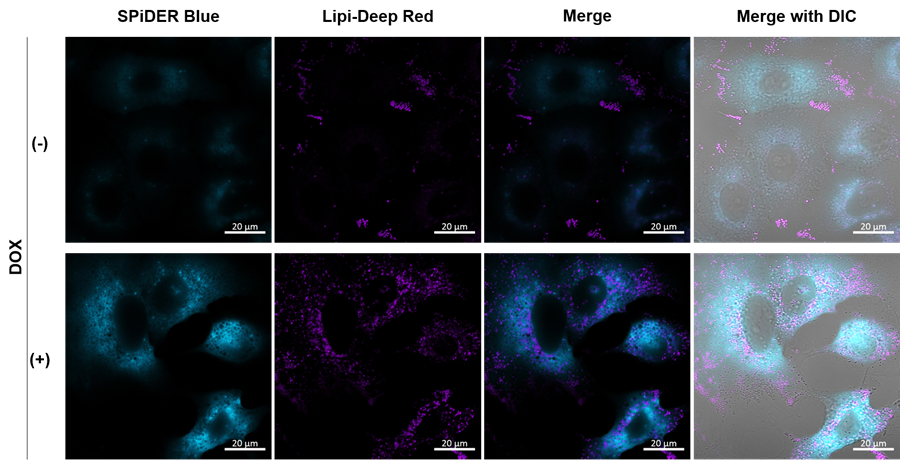
Doxorubicin処理により老化誘導したA549細胞と通常細胞を用いて、老化細胞における脂肪滴蓄積のイメージング解析を行った。老化マーカーとしてSA-β-GalをCellular Senescence Detection Kit - SPiDER Blue, 脂肪滴をLipi-Deep Redで検出した。
[検出条件] SPiDER Blue 検出波長: 405 nm (Ex), 400–550 nm (Em), 1.0%, 600V Lipi-Deep Red 検出波長: 633 nm (Ex), 650–700 nm (Em), 1.0%, 650V
*事前に、通常培地で培養した細胞 と、DOX 処理 (0.2 μM DOX 3 days → 通常培地 3 days) した細胞を準備 1. A549 細胞をμ-slide 8 well plate (ibidi 社) に播種し、37℃ CO2 インキュベーターで一晩培養した。(1 x 105 cells/ml の細胞懸濁液を200 µl 入れた) 2. 上澄みを取り除き、PBS で1回洗浄後、4% パラホルムアルデヒド (PFA) / PBS 溶液を添加し、室温で30 分間固定化した。 3. 上澄みを取り除き、細胞をPBS で1 回洗浄した。 4. Assya bufferで調製した15 μM SPiDER Blue + 0.1 µM Lipi-Deep Red を添加し、 37℃で30 分間インキュベートした。 *5% CO2 インキュベーターは使用しない 5. 上澄みを取り除き、PBS で1 回洗浄後、PBS を200 µl添加し共焦点レーザー顕微鏡 (60 倍率) で観察した。
|
|||